제품소개
|
제품명 |
고양이. 아니요. |
투기. |
|
면역침전 키트(단백질 A 아가로스) |
G2215-50T |
50 T |
제품 설명/소개
IP 또는 Co-IP는 특정 항체와 항체에 결합하는 배지(예: Protein A/G Agarose 또는 Protein A/G Magrose)를 사용하거나 직접 특정 항체(예: 아가로스 또는 자기 비드)와 결합된 배지를 사용한 다음 원심분리 또는 자력을 사용하여 복잡한 단백질 샘플에서 항원-항체 복합체를 분리하여 표적 단백질의 분리 및 정제 목적을 달성합니다. 사용되다 웨스턴 블롯 또는 질량 분석법의 경우. 단백질 A는 황색포도상구균에서 발견되는 세포벽 표면 단백질로 분자량이 42kDa입니다. 단백질 G는 연쇄구균 박테리아 유형 C 또는 G에 의해 발현되는 면역글로불린 결합 단백질입니다. 단백질 A와 단백질 G는 기능적으로 유사하며 포유동물 면역글로불린(Ig)에 특이적으로 결합할 수 있습니다. 아가로스에 결합된 적절한 변형이 있는 재조합 단백질 A 및 G는 면역침전 또는 항체 정제에 사용될 수 있습니다. 단백질 A 아가로스는 인간 IgG1, IgG2, IgG4, 마우스 IgG2a, IgG2b의 면역 침전에 적합하고, 단백질 G 아가로즈 비드는 인간 IgG1, IgG2, IgG3, IgG4, 마우스 IgG1, IgG2a, IgG2b, IgG3의 면역 침전에 적합합니다. 쥐 IgG1, IgG2a, IgG2b, IgG2c 다클론 항체. (구체적인 정보는 표 I 참조)
본 제품은 자체 개발 및 생산된 Protein A 표지 아가로스를 사용하여 시중의 유사 제품에 비해 보다 효율적으로 항체와 결합하고 비특이적 결합률이 낮으며 최적화된 완충액과 함께 사용하면 편리하고 효율적입니다. 면역침전 실험을 위해; 이는 세포 용해물, 세포 분비 상청액, 혈청, 복수 등과 같은 샘플에서 표적 단백질의 분리 및 정제에 널리 사용될 수 있습니다. 이 키트는 표적 단백질을 용출하기 위한 두 가지 용리 방법(변성 용리 및 산 용리)을 제공합니다. 특히 산 용출에는 항체의 경쇄 및 중쇄가 포함되지 않으므로 항체의 중쇄 및 경쇄 간섭 문제를 효과적으로 해결할 수 있습니다. 면역침전 및 단백질 면역블로팅 실험의 사슬.
제품정보
|
형질 |
설명 |
|
제품 내용 |
특정 보호 완충액에 50%(v/v) 아가로스 |
|
비즈 구조 |
6% 가교 아가로스 |
|
결합단백질 |
단백질 A |
|
단백질의 MW |
~25 kDa(단백질 A) |
|
결합 단백질 용량 |
>ml 구슬 당 1mg 마우스 항체 |
|
특성 |
생쥐, 인간, 쥐, 염소, 양, 소를 포함한 다양한 종의 항체 |
|
비드 직경 |
30~150 μm |
|
용출 방법 |
산 또는 1x SDS‐PAGE 로딩 버퍼를 사용한 용출(감소) 참고: 1x SDS‐PAGE 로딩 완충액(환원)으로 용출되면 항체의 중쇄(~50kDa) 및 경쇄(~25kDa)가 변성되어 아가로스 비드에서 방출됩니다. |
|
응용 |
IP, Co-IP, 단백질 정제 |
보관 및 배송 조건
젖은 얼음으로 배송하십시오. 5×SDS-PAGE 로딩 버퍼(축소)는 -20도에서 다른 것들은 2-8도에서 12개월간 보관해야 합니다.
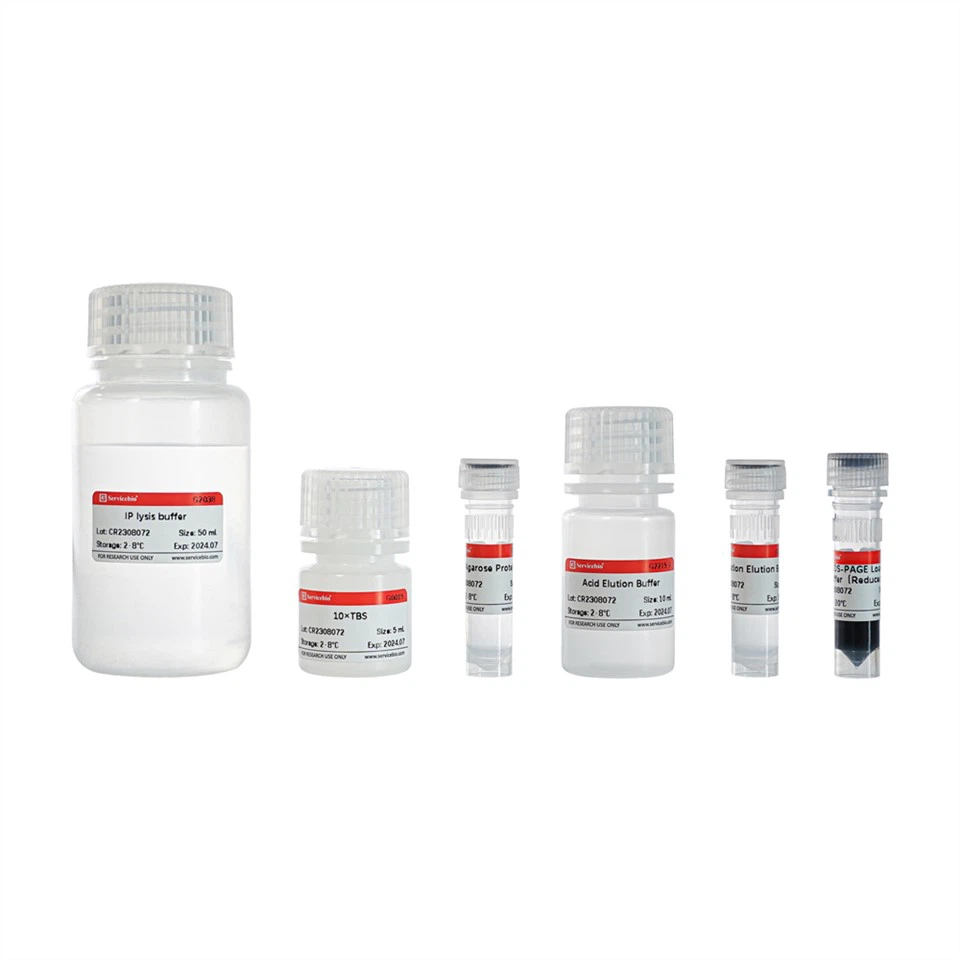
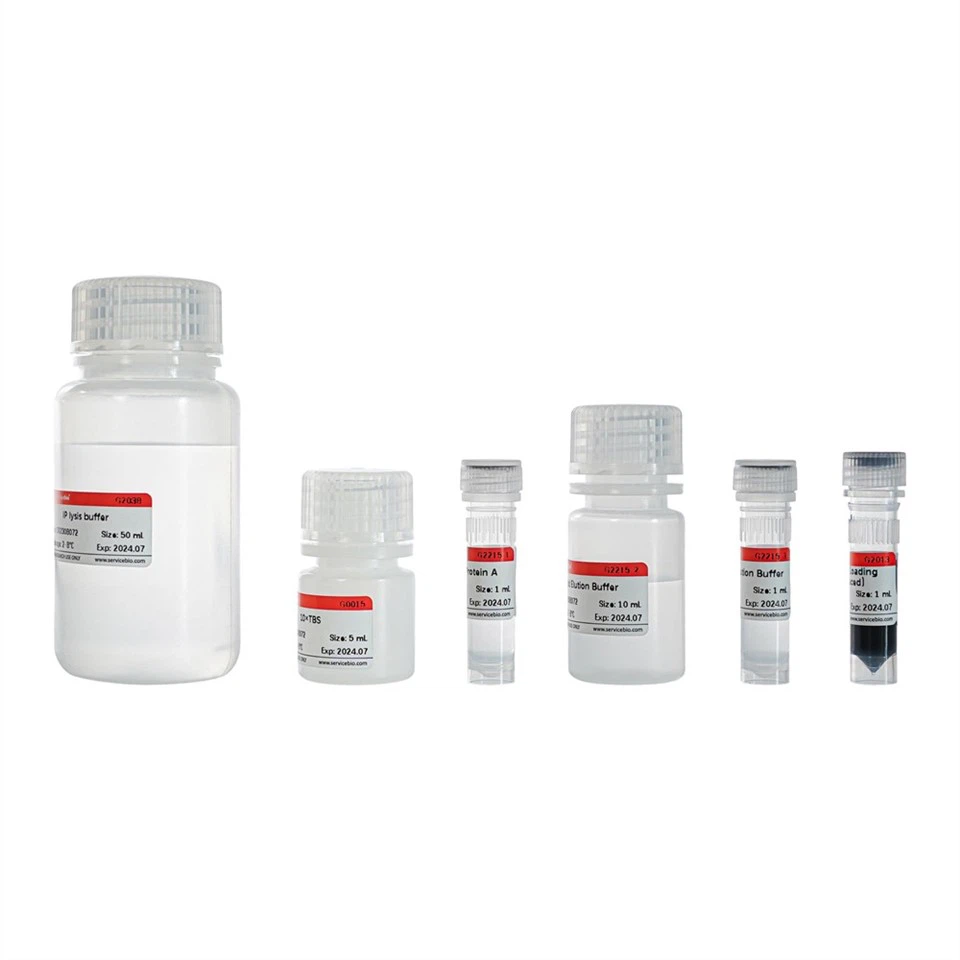
제품 구성요소
|
구성요소 번호 |
요소 |
G2215-50T |
보관온도 |
|
G2038 |
IP 용해 완충액 |
50mL |
2-8도 |
|
G0015 |
10×TBS |
5mL |
2-8도 |
|
G2215-1 |
스웨아가로스 단백질 A |
1mL |
2-8도 |
|
G2215-2 |
산성 용출 완충액 |
10mL |
2-8도 |
|
G2215-3 |
중화 용출 버퍼 |
1mL |
2-8도 |
|
G2013 |
5x SDS-PAGE 로딩 버퍼(감소) |
1mL |
-20도 |
|
수동 |
1개 |
||
추가 시약 필요
|
제품명 |
고양이. 숫자 |
투기. |
|
50×칵테일 프로테아제 억제제 |
G2006-250UL |
250 μL |
|
PBS, 1×(인산염 완충 식염수) |
G4202-500ML |
500mL |
분석 프로토콜/절차
1. 키트 준비
a) 아래 표를 참조하여 샘플당 용해물 100-500 μL의 비율로 관련 시약을 준비합니다.
|
단계 |
필요한 솔루션 |
볼륨 |
볼륨 |
|
세포 용해 및 준비 |
칵테일 프로테아제 억제제를 함유하는 IP 용해물 |
100 μL |
500 μL |
|
지적 재산권 |
스웨아가로스 단백질 A |
4 μL |
20 μL |
|
세 번 씻으세요 |
1×TBS |
100 μL |
500μL |
|
산 용출 및 중화 |
산성 용출 완충액 |
20 μL |
100 μL |
|
중화 완충액 |
20 μL |
100 μL |
|
|
변성 용출 |
1x SDS-PAGE 로딩 버퍼(감소) |
20 μL |
100 μL |
b) 프로테아제 억제제를 함유한 IP 용해물 준비: 위 표를 참조하여, 용해를 위해 0.5-1백만 세포당 프로테아제 억제제를 함유한 IP 용해물 {{0}} μL를 사용합니다. IP 용해물을 50x 칵테일 프로테아제 억제제(G2006-250UL 권장)와 50:1의 비율로 혼합합니다. 예를 들어 IP 용해물 1mL에 20μL의 50x 칵테일 프로테아제 억제제를 추가한 다음 1mL의 50x 칵테일 프로테아제 억제제를 추가합니다. 프로테아제 억제제를 함유한 IP 용해물이 얻어질 것입니다; 억제제가 포함된 준비된 IP 용해물은 얼음 욕조에 넣거나 4도에 놓아야 합니다.
c) 참고: 면역침강의 표적 단백질이 인산화 또는 아세틸화 변형과 관련된 경우 포스파타제 억제제 또는 탈아세틸화효소 억제제를 추가해야 합니다(자체 제공). 억제제를 함유한 IP 용해물은 사용하기 전에 준비해야 하며, 이후 사용을 위해 냉동하거나 보관해서는 안 됩니다.
d) 1×TBS의 제조: 10×TBS 완충액을 초순수로 희석하여 1×TBS로 한다. 예를 들어 초순수 9mL에 10×TBS 버퍼 1mL를 첨가하고, 이는 잘 섞은 후 1×TBS 버퍼입니다.
e) 1x SDS-PAGE 로딩 버퍼(환원) 준비: 적당량의 5x SDS-PAGE 로딩 버퍼(환원)를 초순수로 5배 희석하여 1x SDS-PAGE 로딩 버퍼(환원)를 만듭니다. 예를 들어, 5x 단백질 완충액(환원)의 0.2mL를 1x SDS-PAGE 로딩 완충액(환원)인 0.8mL 초순수와 혼합합니다.
2. 항원 샘플 준비
면역침전 또는 면역침강 실험은 샘플이 용해된 직후에 수행되어야 합니다. 그렇지 않은 경우 샘플은 -20도 또는 -80도에서 냉장고에 보관할 수 있지만 냉동 및 해동은 단백질-단백질 상호작용에 영향을 미칠 수 있습니다. 모든 샘플 용해 단계는 단백질 분해를 최소화하기 위해 얼음조 또는 4도에서 작동해야 하며, 후속 검출을 위해 샘플을 준비한 후 일정량의 샘플을 입력 또는 총계로 취해야 합니다. 웨스턴 블롯.
조직 샘플의 경우:
a) 조직은 미리 차가운 PBS(G4202 권장)로 헹구어 과도한 혈액을 완전히 제거해야 합니다. 얼음 위의 균질화기에서 무게를 측정하고 작은 조각으로 다집니다.
b) 조직의 10-20 mg당 100-200 μL의 비율로 프로테아제 억제제가 포함된 IP 용해물을 추가하거나 더 높은 농도의 단백질이 필요한 경우 IP 용해물의 양을 줄입니다.
c) 유리 균질기 또는 휴대용 균질기를 사용하여 균질화하거나 자체 개발한 KZ-III-F 저온 분쇄기를 사용하여 전체 분쇄합니다.
d) 균질액을 1.5 mL 원심분리 튜브에 옮기고 흔들어 섞은 후 30분 동안 얼음에 담그고 10분마다 피펫으로 불어서 조직 세포가 완전히 용해되도록 반복했습니다.
e) 12,000 xg에서 4도에서 5분간 원심분리하고 침전물을 버리고 후속 면역침전 또는 면역침전 실험을 위해 상층액을 흡인합니다.
부착 세포 샘플의 경우:
a) 필요한 경우 세포를 PBS로 2-3회 세척하고 마지막에 남은 액체를 완전히 흡수할 수 있습니다.
b) 세포 스크레이퍼 또는 트립신 소화로 세포를 긁어내어 세포를 완전히 현탁시키고, 1.5 mL 원심분리 튜브에 모아서 1,000 xg에서 4도에서 5분간 원심분리하고, 상층액을 버립니다. 세포 침전물을 수집합니다.
c) 0.5-1백만 개의 세포당 프로테아제 억제제를 함유한 IP 용해물 {{0}}μL를 첨가합니다(6-웰 플레이트의 1웰에 해당). 세포를 완전히 용해시키기 위해 적절하게 불어넣고 얼음욕을 3-5분 동안 하고, 완전히 용해된 후에 뚜렷한 세포 침전이 없어야 합니다. 세포의 양이 더 많으면 세포를 0.{6}}백만 개의 세포/튜브로 나누어 완전히 용해시키는 것이 좋습니다.
d) 충분한 용해 후 12,000 xg에서 4도에서 5분간 원심분리하고 침전물을 버리고 후속 면역침전 또는 면역침전 실험을 위해 상청액을 흡인합니다.
정지 세포 샘플의 경우:
a) 침전물을 수집하기 위해 1,000 xg에서 5분간 4도에서 원심분리합니다. 필요한 경우 PBS로 한 번 세척한 다음 잔여 액체를 흡인하고 부드럽게 소용돌이시켜 세포를 최대한 분산시킵니다.
b) 0.5-1백만 개의 세포당 프로테아제 억제제를 함유한 IP 용해물 {{0}}μL를 첨가합니다(6-웰 플레이트의 1웰에 해당). 세포를 완전히 용해시키기 위해 적절하게 불어넣고 3-5분 동안 얼음 욕조에 담그십시오. 세포의 양이 더 많으면 세포를 0.{6}}백만 개의 세포/튜브로 나누어 완전히 용해시키는 것이 좋습니다.
c) 얼음욕조에서 5분간, 12000g, 4도에서 5분간 원심분리한 후 상등액, 즉 전체 단백질 용액을 취하여 후속 면역침전 또는 면역침전 실험 등에 사용할 수 있습니다.
박테리아 또는 효모 샘플의 경우:
a) 세균 또는 효모 용액 1 mL를 취하여 원심분리하여 상청액을 제거한다. 필요한 경우 세포를 PBS로 한 번 세척하고 마지막에 남은 액체를 완전히 흡수할 수 있습니다. 튜브 바닥을 부드럽게 소용돌이치거나 가볍게 움직여 세포를 최대한 분산시킵니다.
b) 프로테아제 억제제가 포함된 IP 용해물 100-200μL를 첨가하고 박테리아나 곰팡이가 완전히 분산되도록 가볍게 불어줍니다.
c) 10분 동안 얼음욕조에서 더 나은 용해를 위해 박테리아와 효모를 각각 라이소자임과 벽 파괴 효소(자체 제공)로 소화한 다음 프로테아제 억제제가 포함된 IP 용해물로 용해할 수 있습니다.
d) 12,000 xg에서 4도에서 5분간 원심분리하고 침전물을 버리고 후속 면역침전 또는 면역침전 실험을 위해 상층액을 흡인합니다.
3. 아가로즈 준비
a) SweAgarose Protein A 비드를 부드럽게 재현탁하여 가능한 한 균일한 비드 분산액을 형성하고, 시료 500ul마다 잘 혼합된 비드 분산액 20ul를 추가하고, 적절한 양의 아가로스 비드를 EP 튜브를 청소하고 1x TBS를 최종 부피 0.5mL에 추가합니다(각 샘플에 대한 비드 분산액 20ul는 예를 들어 다음 면역 침전 단계에서 사용됩니다).
b) 비드를 부드럽게 다시 부유시키고, 6도에서 원심분리하고,000×g, 4도에서 30초 동안 조심스럽게 상층액을 제거하고 위의 단계를 2회 반복합니다.
c) 초기 비드 분산액의 부피에 따라 비드를 1x TBS로 재현탁했습니다.
4. SweAgarose Protein A 비드에 결합하는 항체
a) 항체 제조: 항체 지침에서 권장하는 희석 비율에 따라 항체를 1x TBS로 희석하여 항체 작동 용액을 제조하거나, 최종 농도가 5-50 ug/mL인 항체 작동 용액으로 항체를 제조합니다. , 얼음 위에서 준비할 수 있음; 선택 사항: 동일한 항체 종의 일반 IgG를 사용하여 동일한 희석 비율 또는 최종 농도 5-50 ug/mL로 일반 IgG 작업 용액을 준비하거나, 비특이적 결합을 제거하거나 음성 대조군으로 사용합니다. 동일한 종의 정상 IgG는 후속 면역침강에 사용되는 항체가 마우스 IgG인 경우 이 단계에서 적당량의 정상 마우스 IgG를 1x TBS로 희석하여 배경을 줄이거나 음성 대조군으로 사용할 수 있음을 의미합니다.
b) 항체 흡착: 3단계에서 제조한 SweAgarose Protein A 비드를 6,000 xg, 4도에서 30초간 원심분리하여 분리하고, 상등액을 흡인한 후, 항체 작업 용액 또는 일반 IgG 작업 용액 500 μL를 첨가하고, 재현탁합니다. 그런 다음 턴오버 믹서에서 실온에서 15-60분 동안 배양합니다.
참고: 3단계에서 준비된 SweAgarose Protein A 비드를 적절한 양의 항체 또는 정상 IgG와 함께 직접 배양하는 것도 가능합니다.
c) 비드 분리 및 세척: 인큐베이션된 비드를 6,000 xg, 4도에서 30초 동안 원심분리기로 분리하고, 상청액을 흡인하고, 500μL의 1×TBS를 추가하고, SweAgarose Protein A 비드를 부드럽게 불어서 재현탁시킵니다. 피펫, 원심분리기 6,000 xg, 4도에서 30초, 상층액 제거, 세척을 반복 3회 반복하고 초기 용량과 동일한 양의 1×TBS로 비드를 재현탁합니다.
참고: 배양 및 세척 중에 구슬이 뭉치거나 벗겨지는 경우 이는 정상적인 현상이며 실험 결과에 영향을 미치지 않습니다.
5. 면역침전(IP):
a) 비특이적 결합 제거(선택 사항): 4단계에서 준비한 정상 IgG에 결합하는 SweAgarose Protein A 비드를 샘플과 함께 4도에서 60분간 배양한 후 6도에서 원심분리기로 분리합니다.000 4도에서 30초 동안 xg, 상층액은 후속 실험에 사용됩니다. 이 단계의 목적은 정상 IgG에 비특이적으로 결합하는 단백질을 제거하는 것입니다.
b) 항체 또는 정상 IgG와 결합된 SweAgarose 단백질 A 비드와 시료의 인큐베이션: 단백질 시료 500ul당 비드 현탁액 20ul의 비율로 항체 또는 정상 IgG와 결합된 SweAgarose 단백질 A 비드를 추가하고 한쪽에 놓습니다. 진동 셰이커 또는 로터리 믹서를 사용하여 실온에서 2시간 동안 배양하거나 4°C에서 하룻밤 동안 배양합니다.
참고 1: 배양 및 세척 중에 구슬이 뭉치거나 벗겨지는 경우 이는 정상적인 현상이며 실험 결과에 영향을 미치지 않습니다.
참고 2: 또는 적절한 양의 항체 또는 정상 IgG를 실온에서 1-2시간 동안 또는 4도에서 하룻밤 동안 시료와 함께 배양한 다음 10-20μL의 아가로스 비드 현탁액을 첨가할 수 있습니다. 그리고 실온에서 60분 동안 배양하였다.
c) 원심분리기: 배양 후 6000 xg에서 4도에서 30초 동안 원심분리하여 상청액을 제거합니다.
참고: 면역 침전의 효과를 테스트하기 위해 상층액의 일부를 유지하십시오.
d) 세척: 500ul의 1×TBS를 첨가하고, 재현탁된 비드를 피펫으로 부드럽게 불어넣고, 6도에서 원심분리하고,000 xg로 4도에서 30초 동안 상등액을 제거하고 세척을 3회 반복합니다.
참고: 세척 완충액의 OD280을 분석하여 세척이 완료되었는지 확인할 수도 있습니다. OD280이 0.05보다 큰 경우 세척 횟수를 적절하게 늘려야 합니다.
6. 용출
목적 단백질의 특성과 후속 실험의 요구 사항에 따라 다음 방법 중 하나를 선택하여 용출할 수 있습니다.
a) 변성 용출 방법: 이 방법으로 용출된 샘플은 SDS-PAGE에 적합합니다. 원심분리 후 1× Protein Sampling Buffer(Reduced) 25 µL를 튜브에 넣고 95도에서 5분간 가열한 후 원심분리하여 Western blot 검출을 위한 상층액을 수집합니다.
b) 산 용출: 이 방법으로 용출된 샘플은 원래의 생물학적 활성을 유지하며 사후 기능 분석에 사용할 수 있습니다. 원심분리 후 튜브에 Acid Elution Buffer 20 µL를 넣고 잘 섞은 후 실온에서 10분간 배양한 후 원심분리하여 상층액을 새 EP 튜브에 모으고 즉시 Neulization Elution Buffer 2 µL를 넣어 pH를 조절합니다. 용출된 생성물을 중성으로 만들어 사후 기능 분석에 사용할 수 있습니다.
참고: 사용자는 원하는 양에 따라 추가되는 용출 버퍼의 양을 조정할 수 있습니다.
메모
1. SweAgarose Protein A를 키트에 -20도에서 보관하거나 반복적으로 동결 및 해동하지 마십시오. 그렇지 않으면 자기 비드의 성능에 영향을 미치고 불필요한 실험 오류가 발생할 수 있습니다.
2. 면역침전 절차를 수행하기 전에 이 지침을 주의 깊게 읽으십시오.
3. 면역침전된 목적 단백질이 인산화 또는 아세틸화 변형을 수반하는 경우에는 적절한 포스파타제 억제제 및 데아세틸라제 억제제를 제공해야 한다.
4. 비드를 pH 6-8로 유지하고 고속 원심분리, 건조 또는 동결을 피하십시오. 이는 비드 응집을 유발할 수 있습니다.
5. 사용하기 전에 비드를 완전히 혼합해야 하며, 혼합 작업은 부드럽게 이루어져야 하며, 항체의 변성을 방지하기 위해 격렬한 소용돌이나 흔들림을 가해서는 안 됩니다.
6. 면역침강에는 양성 및 음성 대조군(SweAgarose Mouse IgG)을 권장합니다.
7. 단백질 샘플은 수집 후 가능한 한 빨리 정제해야 하며, 단백질 분해 또는 변성을 늦추기 위해 항상 4도 또는 얼음조에 보관해야 합니다.
8. 산성 용출과 함께 사용할 때 아가로스 비드가 모일 수 있습니다. 이는 정상적인 현상이며 자기 비드의 정상적인 사용에 영향을 주지 않습니다.
9. 본 제품은 전문가의 과학적 연구용으로만 제한되어 있으며, 임상진단이나 치료, 식품, 의약품 용도로 사용하거나 일반 거주지에서 보관할 수 없습니다.
10. 실험실 작업복, 보안경, 장갑 등 적절한 보호복을 착용하십시오.
11. 다양한 일반 공급원 및 하위 유형의 항체에 대한 단백질 A 및 단백질 G의 결합 능력은 표 I에 나와 있습니다.
표 1
|
종 |
이그 |
단백질 A |
단백질 G |
총 Ig |
단백질 A |
단백질 G |
|
인간 |
IgG1 |
++++ |
++++ |
인간 |
++++ |
++++ |
|
IgG2 |
++++ |
++++ |
생쥐 |
+++ |
+++ |
|
|
igG3 (영문) |
- |
++++ |
쥐 |
+/- |
++ |
|
|
이그G4 |
++++ |
++++ |
토끼 |
++++ |
+++ |
|
|
이가 |
++ |
- |
염소 |
- |
++ |
|
|
이그디 |
++ |
- |
닭 |
- |
+ |
|
|
igE (영문) |
++ |
- |
암소 |
++ |
++++ |
|
|
이그엠 |
++ |
- |
기니피그 |
++++ |
++ |
|
|
생쥐 |
IgG1 |
+ |
++++ |
햄스터 |
+ |
++ |
|
IgG2a |
++++ |
++++ |
말 |
++ |
++++ |
|
|
IgG2b |
+++ |
+++ |
돼지 |
+++ |
+++ |
|
|
igG3 (영문) |
++ |
+++ |
양 |
+/- |
++ |
|
|
이그엠 |
+/- |
- |
++++:강력한 Bing |
|||
|
쥐 |
IgG1 |
- |
+ |
++~+++:중간 바인딩 |
||
|
IgG2a |
- |
++++ |
+:약한 결합 |
|||
|
IgG2b |
- |
++ |
+/-:약함 또는 바인딩 없음 |
|||
|
IgG2c |
+ |
++ |
-:바인딩 없음 |
|||
|
IgM |
+/- |
- |
||||
연구용으로만 사용하세요. 진단 또는 치료 절차에 사용하지 마십시오!
인기 탭: 면역침전 키트(단백질 a agarose), 중국 면역침전 키트(단백질 a agarose) 제조업체, 공급업체, 공장